Año: 2025 Volumen: 7
Las enfermedades cardiovasculares ateroscleróticas (ECVA) suponen la principal causa de mortalidad a nivel mundial. La principal intervención para su tratamiento, es la disminución del colesterol de las lipoproteínas de baja densidad (c-LDL). Sin embargo, pese al tratamiento, sigue existiendo un riesgo cardiovascular residual debido entre otros factores, a la lipoproteína (a) (Lp(a)), constituyendo un factor de riesgo independiente para el desarrollo de enfermedad cardiovascular (ECV) (1,2). A pesar de haberse establecido su asociación con la ECV desde hace décadas, ha sido en los últimos años cuando se ha incrementado el interés por su estudio (3,4). Diferentes estudios epidemiológicos y genéticos asocian niveles elevados de Lp(a) con la ECVA (enfermedad coronaria, accidente cerebrovascular isquémico y enfermedad arterial periférica) y la estenosis de la válvula aórtica (1,3-6). Varios trabajos han asociado la Lp(a) con un mayor riesgo de eventos cardiovasculares mayores (MACE), de forma independiente a otros biomarcadores (c-LDL y proteína C reactiva de alta sensibilidad), pudiendo predecirse el riesgo de MACE a 20 años en una única determinación conjunta, siendo mayor el riesgo cuando éstos tres valores se encuentren altos (7,8). Se estima que cerca de 1 de cada 5 personas en el mundo presentan niveles elevados de Lp(a) (≥100-125 nmol/L, aproximadamente ≥50mg/dL). Su prevalencia es muy superior a la hipercolesterolemia familiar heterocigótica, un factor de riesgo bien establecido de enfermedad cardiovascular aterosclerótica (ECVA), que tiene una prevalencia mundial de 1 de cada 311 personas (3,4). Entre el 80-91% de la concentración plasmática de Lp(a) está determinada genéticamente (gen LPA)(1,3,4,9), por lo que en general los niveles plasmáticos permanecen estables a lo largo de la vida, sin embargo se ha observado variabilidad según población. Así, la población negra es la que presenta mayores valores de Lp(a), seguida en orden decreciente por sudasiática, blanca y china (medianas de 75, 31, 19 y 16 nmol/L, respectivamente), aunque parece que el riesgo de ECVA permanece similar entre las diferentes poblaciones (9). Además, la concentración de Lp(a) es ligeramente mayor en mujeres que en hombres (3,5). Aparte de los genéticos existen otros factores que, aunque en menor medida, pueden afectar a la concentración de Lp(a). Las hormonas que afectan al metabolismo de lipoproteínas pueden influir en la concentración (5), como en las alteraciones tiroideas y en el caso del embarazo y la menopausia, donde se sugiere que el estradiol endógeno puede ser el responsable del aumento en los valores de Lp(a). Las alteraciones renales graves y enfermedades inflamatorias crónicas aumentan la concentración de Lp(a), mientras que las alteraciones hepáticas graves la pueden disminuir (3,4). Las intervenciones en el estilo de vida, el ejercicio físico y la dieta tienen un impacto mínimo en la modificación de la concentración de Lp(a), aunque parece que una dieta baja en hidratos de carbono y rica en grasas saturadas y nueces, podría disminuir los valores aproximadamente un 10-15% (3-5,10). La Lp(a) está compuesta por una lipoproteína (similar al LDL) que contiene la apoproteína B100 (apoB100) y la apoproteína (a) (apo (a)). La apo (a) está formada por los dominios kringle IV, kringle V y proteasa inactivo. El dominio Kringle IV es el que determina la longitud y el peso molecular total de la isoforma de la apo(a), estando inversamente relacionado con el nivel plasmático de Lp(a), así las isoformas cortas son las que presentan mayor concentración plasmática de Lp(a) (1,3,4,9). Como lipoproteína, transporta colesterol, triglicéridos, fosfolípidos (incluyendo fosfolípidos oxidados), y otras apoproteínas (1,3,4,9). La Lp(a) parece ser 6 veces más aterogénica que el c-LDL a pesar de la mayor abundancia de partículas c-LDL en plasma, debido a dos componentes pro-aterogénicos, la lipoproteína similar a LDL y la apo(a). Así, los efectos proaterogénicos, proinflamatorios y protrombóticos/antifibrinolíticos de la Lp(a) se han asociado al incremento en el riesgo cardiovascular de esta lipoproteína (1,4,9): La Lp(a) es un factor de riesgo de ECV. El impacto de los niveles de Lp(a) en el riesgo de ECV está condicionado por el riesgo basal del individuo. Se recomienda la medición de los niveles de Lp(a) para una evaluación integral del riesgo de ECV al poder ser subestimado si no se considera, ya que pueden estar presentes valores elevados de Lp(a) a pesar de valores normales de c-LDL y triglicéridos (3-6). Existen coeficientes de corrección del riesgo calculado mediante la escala de riesgo cardiovascular SCORE 2 en función de los niveles de Lp(a). Además, se dispone de calculadoras online del riesgo cardiovascular hasta los 80 años, que incorporan los niveles de Lp(a) (3, 10). Según la concentración sanguínea de Lp(a) se distinguen las siguientes categorías (4,5): Modificada de: (4) Varias guías de práctica clínica recomiendan la medición de la Lp(a) al menos una vez en la vida adulta, ya que en general los niveles de Lp(a) no varían a lo largo de la vida (3,4,6). Existen determinadas situaciones que podrían justificar una nueva determinación como: menopausia (6), insuficiencia renal avanzada, síndrome nefrótico, si la determinación se realizó en el embarazo, disfunción hepatocelular, hipo/hipertiroidismo, sepsis o procesos inflamatorios importantes, o cuando los valores obtenidos se encuentren cercanos a los límites (3). Es especialmente importante su determinación en la ECV precoz en ausencia de factores de riesgo tradicionales, así como en, historial familiar de elevación de Lp(a), hipercolesterolemia familiar, pobre respuesta a estatinas y en personas con riesgo moderado o cerca de los umbrales de decisión del tratamiento para mejorar la clasificación del riesgo (3,6). Actualmente no hay tratamiento específico para la reducción de los niveles elevados de Lp(a). Varios fármacos indicados para la reducción del c-LDL, pueden tener efecto en la reducción de los niveles de Lp(a). Entre ellos se encuentran (1-4): Se encuentran en investigación nuevos fármacos dirigidos específicamente a la reducción de los niveles de Lp(a) teniendo como diana el ARNm o la formación de la Lp(a) (3,4). A pesar de haberse establecido su asociación con el riesgo de ECV y mayor aterogenicidad que c-LDL, debido a que la concentración de la Lp(a) en plasma es relativamente baja, se desconoce si su reducción disminuirá el riesgo progresión o de nuevos eventos de ECVA y estenosis de la válvula aórtica, ni se conocen estudios que demuestren el beneficio clínico de su reducción o el nivel de reducción que generaría beneficio (2,3,6). En análisis ad hoc de los estudios FOURIER (evolocumab) y ODYSSEY OUTCOMES (alirocumab) se observa que en pacientes con Lp(a) basal alta el beneficio absoluto fue mayor y sugiere que parte del beneficio clínico total podría estar mediado por la reducción de Lp(a), no solo por los niveles de c-LDL (11,12). Además de niveles elevados de Lp(a), se requiere que concurran otros factores de riesgo adicionales. Por ello, no todos los individuos con niveles plasmáticos de Lp(a) elevados, van a desarrollar ECV (4). En la revisión de este artículo ha participado: Dr. Alejandro I. Pérez Cabeza. Médico especialista en Cardiología. Hospital Univiersitario Virgen de la Victoria, Málaga. Epidemiologia y factores que explican su variabilidad
Mecanismos patogénicos
Valores, medidas y recomendaciones sobre cuándo medir la Lp(a)
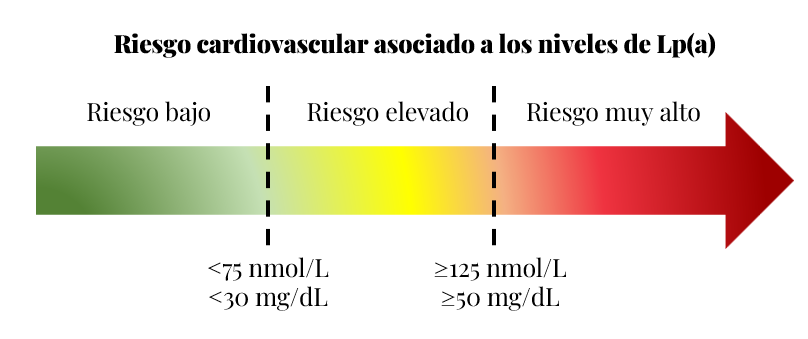
Tratamiento de la Lp(a)
BIBLIOGRAFÍA
Última modificación: 27-11-2025

