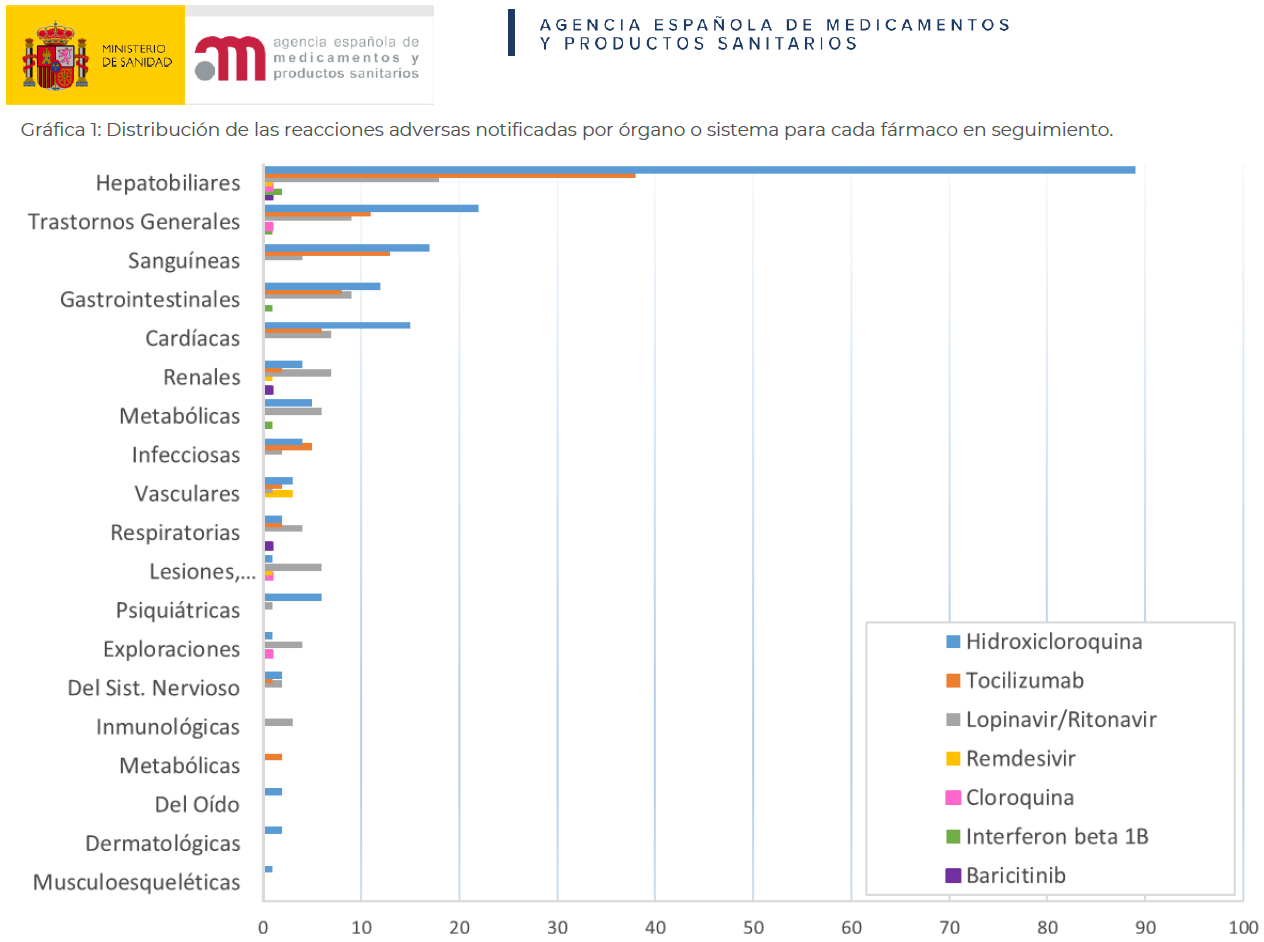
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha publicado el documento titulado “Sospechas de reacciones adversas notificadas con tratamientos utilizados en COVID-19” que recoge las notificaciones enviadas por los profesionales sanitarios al Sistema Español de Farmacovigilancia, en su mayoría a través de los centros autonómicos correspondientes, entre el 1 de marzo y el 3 de mayo de 2020. En la actualidad no hay ningún tratamiento autorizado indicado para la COVID-19. Se están investigando algunos, de los que se están revisando los siguientes: remdesivir, lopinavir/ ritonavir, hidroxicloroquina, cloroquina, tocilizumab, sarilumab, ruxolitinib, siltuximab, baricitinib, anakinra, interferón beta-1B e interferón alfa-2B. Se trata de medicamentos autorizados en otras indicaciones o de nuevo desarrollo, por lo que en ocasiones se usan con pautas de administración diferentes a las autorizadas; y, en pacientes con COVID-19, que pueden presentar características diferentes a los que utilizan estos fármacos para las indicaciones autorizadas, lo que puede afectar al perfil de reacciones adversas. Considerando las limitaciones expuestas anteriormente y que la información de seguridad disponible es muy escasa, las notificaciones recibidas muestran, entre otros, los siguientes hallazgos: - Arritmias cardíacas: Se han notificado 13 casos, en 12 de los cuales el tratamiento era hidroxicloroquina. - Trastornos psiquiátricos: Se han notificado 7 casos, 6 de ellos graves, en pacientes que recibieron tratamiento con hidroxicloroquina. - Trastornos hepáticos: Se han notificado 95 casos en los que interviene hidroxicloroquina (64%) muy frecuentemente en combinación con otros fármacos, como: azitromicina, ceftriaxona, lopinavir/ritonavir y/o tocilizumab. - Trastornos hematológicos: Se han notificado 25 casos, entre ellos 6 casos de hipofibrinogenemia, que recibieron tocilizumab. - Trastornos renales: Se han notificado 12 reacciones adversas renales, todas graves, 6 de las cuales se registraron en pacientes tratados con lopinovir/ritonavir, solo o en combinación con otros medicamentos. - Pancreatitis: Se han notificado 2 casos, con tocilizumab como medicamento sospechoso, además de otra medicación. Para una interpretación adecuada de las sospechas de reacciones adversas, hay que recordar que: las notificaciones de sospecha de reacción adversa, no indican causalidad; los casos notificados no pueden ser utilizados para calcular la incidencia o para estimar la probabilidad de aparición de reacciones adversas del medicamento; y, la evaluación global de todos los casos notificados de una asociación medicamento-reacción adversa, tiene como objetivo únicamente la identificación de potenciales riesgos no conocidos o de cambios en la forma de presentación de las reacciones adversas ya conocidas. Al final se reproduce una gráfica del documento que presenta la distribución de las reacciones adversas notificadas por órgano o sistema para cada fármaco en seguimiento.
Tratamientos para el COVID-19: sospechas de reacciones adversas.
- Detalles
No hay comentarios en el artículo -> “Tratamientos para el COVID-19: sospechas de reacciones adversas. ”
Ratio: 4 / 5